学术动态丨我院郑金刚教授团队合作研究成果入选“2025年度中国科学十大进展”


3月25日,国家自然科学基金委员会发布2025年度“中国科学十大进展”。由我院心脏科郑金刚教授团队与北京大学、山东大学、温州医科大学等顶尖科研团队合作的重大研究成果“发现神经酰胺受体和菌源调控物及其在心血管与代谢性疾病中的作用”成功入选。该研究首次发现并阐明了一种名为“神经酰胺”的脂质分子如何加速动脉粥样硬化,为心血管疾病的精准诊断与治疗,特别是为合并慢性肾脏病的高危人群,带来了突破性的科学见解和干预希望。


动脉粥样硬化是心肌梗死、脑卒中的“元凶”。虽然以他汀类药物为代表的降胆固醇疗法已显著降低了心血管事件,但仍有不少患者在严格降脂治疗的情况下,仍然继续发生动脉粥样硬化的进展,尤其是面对慢性肾脏病合并冠心病的患者时更加显著。医生们常感到“束手无策”——即使血脂“达标”,这部分患者的心血管风险依然居高不下,这被称为“心血管残余风险”。寻找他汀之外的全新干预靶点,已成为全球心血管领域的核心挑战。
一、临床困境的“破局点”:锁定高危患者的“独立风险标志物”
我院心脏科郑金刚教授团队长期深耕于慢性肾脏病合并冠心病的临床与基础研究。面对上述临床“死结”,团队依托其牵头建立的“CRUISE-MET”临床研究队列,对肾功能分期的冠心病患者进行了深入分析。
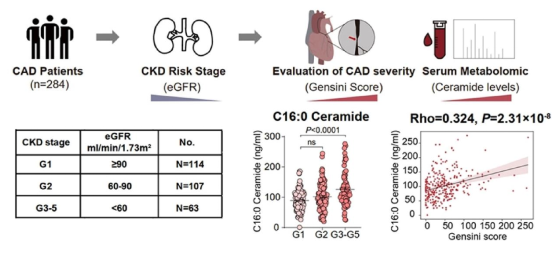
临床研究首次系统性揭示:随着肾功能下降,患者血液中多种“长链神经酰胺”(如C16:0、C18:0)的水平会显著升高。最关键的是,即便完全排除了传统胆固醇、血压、血糖等所有已知危险因素的影响,神经酰胺水平仍与患者冠状动脉病变的严重程度独立相关。这有力地证实,神经酰胺是慢性肾脏病患者心血管风险的、独立于传统因素的新型生物标志物。这一发现,为精准识别最高危人群提供了明确的“标尺”,也意味着干预“残余风险”找到了新的突破口。
二、从临床到机制:首次鉴定神经酰胺的内源性受体并阐明致病通路
临床问题指引了基础研究的方向。通过与合作团队进一步探索:神经酰胺这个“坏脂肪”究竟如何作恶?
研究团队取得了一项里程碑式的发现:首次在国际上鉴定出神经酰胺在人体内发挥作用所必须的两个关键受体蛋白——CYSLTR2和P2RY6,并精确解析了其三维结构。神经酰胺与这两个受体结合,激活细胞内的炎症信号,导致血管损伤和动脉粥样硬化加剧。这项发现从根源上解释了神经酰胺如何致病,并为其设定了明确的药物干预靶点。
三、完成转化医学闭环:临床前研究验证靶向干预的治疗潜力
在明确靶点后,研究在动物模型中验证了其治疗潜力。在模拟人体“慢性肾病合并动脉粥样硬化”的疾病模型中,使用药物阻断CYSLTR2或P2RY6受体后,即便不降低胆固醇,也能显著减轻动脉粥样硬化病变。这证明,针对这一新通路进行干预,是行之有效的治疗新策略,为未来开发专门用于降低心肾共病患者心血管风险的新药,提供了关键依据。
此项研究的成功入选,是国家对“从临床中来,到临床中去”转化医学研究路径的充分肯定。我院郑金刚教授团队通过扎实的临床队列研究,提出了关键科学问题,并为最终的理论验证提供了核心临床证据,是这项突破性成果中不可或缺的一环。我们期待这一源于中国临床实践的原创发现,能早日转化为惠及全球患者的“中国方案”,为攻克心血管疾病这一人类健康首要威胁贡献更多力量。
<团队介绍>
郑金刚,医学博士,主任医师、教授、博士生导师。中日友好医院心脏科主任、国家临床重点专科学科带头人。担任中国老年医学学会共病精准诊疗分会会长、中国民主促进会中央委员会科技医卫委员会副主任、北京医师协会心血管分会副会长等职务。长期致力于慢性肾脏病合并冠心病的临床与基础研究,承担国自然重大研究计划项目和国自然面上项目等国家级、省部级课题16项。牵头开展国内首个全国多中心透析合并冠心病研究(CRUISE前瞻性和回顾性队列研究)和国际首个血栓内溶栓对STEMI高血栓负荷患者预后影响的队列研究(ATTRACTIVE多中心RCT研究)等临床研究。撰写/参编10项国内重要心血管疾病指南/共识。以第一作者/通讯作者在Nature、Circulation、EuropeanHeartJournal等国际权威杂志发表SCI收录论文80余篇,出版专著4部。

















